Экосистемы, 31: 163–167 (2022) https://ekosystems.cfuv.ru
УДК 57.021:57.052:577.29
Инновационный постгеномный подход в борьбе с лавровой листоблошкой Trioza alacris Flor.
Новиков И. А.1, Яцкова Е. В.2, Шармагий А. К.2, Пузанова Е. В.1, Билык А. И.1,
Оберемок В. В.1, 2
- Крымский федеральный университет имени В. И. Вернадского Симферополь, Республика Крым, Россия
i.nowikow2012@mail.ru, 17obruchka@mail.ru, bilyk.ai97@mail.ru, voloberemok@gmail.com
- Ордена Трудового Красного Знамени Никитский ботанический сад – Национальный научный центр РАН Ялта, Республика Крым, Россия vercful@mail.ru, alexander_sharma@mail.ru
В настоящей статье мы описываем эффективность олигонуклеотидных инсектицидов (ДНК-инсектицидов) Алакрис-11 и Лаура-11, а также их смесь в соотношении 1:1, созданных для регуляции численности лавровой листоблошки Trioza alacris Flor., которые основаны на коротких немодифицированных антисмысловых ДНКолигонуклеотидах, нацеленных на 28S рРНК и межгенный транскрибируемый спейсер ITS2 между 5,8S и 28S рибосомальной РНК целевого насекомого соответственно. Опыт проведен на растениях лавра благородного Laurus nobilis L. на Южном берегу Крыма в 2021-2022 годах в трех повторностях. Значительная смертность насекомых отмечена уже на третьи сутки эксперимента для олигонуклеотидного инсектицида Лаура-11, которая составила 67,61±3,09 %. Максимальная смертность насекомых наблюдалась на четырнадцатый день эксперимента и составила для Алакрис-11 95,00±4,42 %, Лаура-11 97,16±2,49 % и их смеси 98,72±1,14 %. После обработки олигонуклеотидами был обнаружен необычный рост содержания РНК-мишени на третий день эксперимента. Для целевого олигонуклеотидного инсектицида Алакрис-11 рост содержания РНК-мишени также наблюдался и в остальные дни эксперимента. Максимальное превышение экспрессии в 7,190,19 раз наблюдалось на четырнадцатый день эксперимента для данного олигонуклеотидного инсектицида. Несовершенно комплементарный фрагмент Проф-11 также вызвал смертность лавровой листоблошки, однако она была невысокой и на четырнадцатый день составила 45,08±0,41 %. Максимальное повышение уровня экспрессии транскрипта предшественника полицистронной рРНК, содержащей межгенный транскрибируемый спейсер ITS2, после применения Проф-11 наблюдалось на четырнадцатый день эксперимента и была в 6,980,21 раз больше, чем в контроле. Отсутствие инсектицидной активности контрольного немодифицированного олигонуклеотида Слог11 свидетельствует об избирательности действия олигонуклеотидных инсектицидов.
Ключевые слова: антисмысловая ДНК, олигонуклеотидные инсектициды, Trioza alacris, лавровая листоблошка, Laurus nobilis, лавр благородный, защита растений.
ВВЕДЕНИЕ
Лавровая листоблошка Trioza alacris Flor. – олигофаг из подотряда Sternorryncha (отряд
Hemiptera), питающийся ценными с хозяйственной точки зрения растениями из семейства Lauraceae: лавром благородным Laurus nobilis, лавром азорским Laurus azorica, лавром канарским Laurus novocanariensis, коричником камфорным Cinnamomum camphora и персеей индийской Laurus indica (http://www.hemiptera-databases.com/psyllist).
В Крыму среди лавровых произрастает только L. nobilis, являющийся одним из древнейших культурных растений, которое помимо промышленного (Zoran et al., 2009) имеет большое декоративное значение (Paparella et al., 2022). Его используют для озеленения садов, парков, скверов, приусадебных участков, применяют в качестве живых изгородей или одиночных посадок (Трикоз, 2017).
T. alacris наносит значительный вред лавру, повреждая молодые листья и побеги и образуя на них ложные галлы. В одном галле может быть более 15 личинок и нимф разного возраста, питающихся соком растений. Свежие галлы имеют бледно-зеленый цвет с розовым или красным оттенком. Поврежденные листья чернеют и засыхают, а растение теряет декоративный вид (рис.1).
ISSN 2414-4738 Published by V. I. Vernadsky Crimean Federal University, Simferopol

Рис. 1. Побеги и листья лавра благородного, поврежденные личинками Trioza alacris
(стрелками обозначены галлы) (фото И. А. Новикова)
Согласно самым ранним исследованиям по использованию ДНК-инсектицидов (также известных как олигонуклеотидные инсектициды, или олинциды) в борьбе с насекомыми подотряда Sternorryncha от 2020 года, этот вид потенциально может быть чувствителен к инсектицидному действию немодифицированных олинцидов (Oberemok et al., 2020; Gal’chinsky et al., 2020; Useinov et al., 2020). Пионерные эксперименты с T. alacris показали достоверные результаты (Novikov et al., 2022). В этой статье мы рассмотрим смертность и измерим содержание РНК-мишени данного вредителя после обработки целевыми олинцидами, а также нецелевыми олигонуклеотидами.
Цель данной работы – изучить инсектицидные свойства ДНК-олигонуклеотидов Алакрис-11 и Лаура-11 в контроле численности насекомого-вредителя – лавровой листоблошки Trioza alacris.
МАТЕРИАЛЫ И МЕТОДЫ
Были разработаны два целевых антисмысловых олигонуклеотида Алакрис-11 (5’–CCA CCG GGT AG–3′) и Лаура-11 (5’–GAC ACG CGC GC–3′), мишенью для которых является межгенный транскрибируемый спейсер ITS2 в составе полицистронной РНК. Для содания антисмысловых олигонуклеотидов использовался GenBank, кроме этого, были разработаны один случайный и один произвольный фрагменты Слог-11 (5’CTG ACT GAC TG3′) и Проф11 (5’GGT CGC GAC GT3′) соответственно.
Олигонуклеотиды синтезировали на автоматическом ДНК-синтезаторе АСМ-800 (БИОССЕТ, Россия) стандартным фосфорамидитным методом на универсальном твердом носителе UniLinker 500Å (ChemGenes, США). Удаление олигонуклеотидов с твердофазного носителя и снятие защитных групп проводили при температуре 55 ºС в течение ночи с использованием концентрированного раствора аммиака. После раствор фильтровали и упаривали в вакууме на ротационном испарителе (Heidolph, Германия). Полученное твердое
Новиков И. А., Яцкова Е. В., Шармагий А. К., Пузанова Е. В., Билык А. И., Оберемок В. В.
вещество растворяли в деионизированной воде до нужной концентрации, измеряя её на спектрофотометре NanoDrop Lite (Thermo Fisher Scientific, США).
Соответствие синтезированных фрагментов ДНК определяли с помощью анализатора BactoSCREEN на базе масс-спектрометра MALDI-TOF (Литех, Россия). Соотношение массы (m) к заряду (z) олигонуклеотидов измеряли в виде положительных ионов с 3гидроксипиколиновой кислотой в качестве матрицы на приборе LaserToFLT2 Plus
(Великобритания) в соотношении 2:1. Теоретическое отношение m/z рассчитывали в программе ChemDraw 18.0.
Полевые эксперименты проводиись на Южном берегу Крыма в Никитском ботаническом саду с июня по сентябрь 2021–2022 года на лавре благородном. Обработку лавра проводили с помощью ручного опрыскивателя раствором олигонуклеотидов в деионизированной воде в концентрации 100 мг/л в трехкратной повторности. Обрабатываемая площадь кроны для каждой повторности составляла 1,5 м2. После обработки олигонуклеотидами эффект от их применения регистрировали с третьего по четырнадцатый день. Смертность насекомых рассчитывали с учетом отношения погибших насекомых к общему количеству насекомых, приходящихся на 10 листьев растения при помощи бинокулярного микроскопа МБС-9 (АО ЛЗОС, СССР).
Для ПЦР-анализа выделяли тотальную РНК из личинок лавровой листоблошки после обработки олигонуклеотидами за каждый учётный день эксперимента, используя реактив ExtractRNA (Евроген, Россия). Экстракция РНК была проведена в трех повторностях. Для синтеза кДНК использовали набор для обратной транскрипции (Синтол, Россия) в соответсвии с протоколом производителя. ПЦР в реальном времени для оценки содержания целевой РНК-мишени проводили с использованием набора SYBR Green Master Mix (Roche,
Швейцария) в соответствии с рекомендациями производителя на амплификаторе Light Cycler 96 (Roche, Швейцария).
В реакции ПЦР использовали два праймера: прямой Алакрис-F (5’GAC CTC GGG CTG TAC G3′) и обратный Алакрис-R (5’CGC TTA TTA ATA TGC TTA AA3′). Температуру отжига праймеров рассчитывали по общепринятой формуле (Marmur, Doty, 1962).
Для статистического анализа стандартную ошибку среднего определяли и оценивали с помощью t-критерия Стьюдента. Для оценки достоверности различий между средними показателями групп использовали непараметрический критерий хи-квадрат Пирсона (χ2) с поправкой Йейтса (GraphPad Software, США).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Измерение соответствия синтезированных олигонуклеотидов, определенное с помощью метода MALDI-TOF, показало, что все олигонуклеотиды соответствуют своей структуре, и полученное соотношение отличается от теоретически рассчитанного не более чем на 10 единиц (табл. 1).
Таблица 1
Результаты анализа синтезированных олигонуклеотидов методом MALDI-TOF
| Олигонуклеотиды | Полученное соотношение m/z | Теоретическое соотношение m/z |
| Алакрис-11 | 3337,28 | 3341,60 |
| Лаура-11 | 3328,73 | 3326,60 |
| Слог-11 | 3332,48 | 3331,60 |
| Проф-11 | 3372,56 | 3372,60 |
| Алакрис-F | 4898,64 | 4896,25 |
| Алакрис-R | 6081,59 | 6089,07 |
164
Значительная смертность личинок лавровой листоблошки от разработанного олинцида Лаура-11 наблюдалась уже на третий день эксперимента после обработки пораженных растений и составила 67,61±3,09 % (χ2=82,9, p<0,001, N=117, dF=1). Также повышенная смертность на третий день наблюдалась и при применении смеси олинцидов Алакрис-11 с Лаура-11 в соотношении 1:1 в растворе и составила 46,86±0,74 % (χ2=44,4, p<0,001, N=207, dF=1). Максимальная смертность личинок лавровой листоблошки наблюдалась на четырнадцатый день проведения эксперимента. При применении олинцида Алакрис-11 смертность составила 95,01±4,42 % (χ2=106,3, p<0,001, N=181, dF=1), для олинцида Лаура-11 97,16±2,49 % (χ2=124,4, p<0,001, N=189, dF=1), а для их смеси – 98,72±1,14 % (χ2=163,7, p<0,001, N=222, dF=1). Отмечено, что олигонуклеотид Проф-11 также проявил повышенную инсектицидную активность против личинок лавровой листоблошки на четырнадцатый день, которая вызвала смертность в 45,08±0,41 % (χ2=28,4, p<0,001, N=177, dF=1). Скорее всего это связано с неполной комплементарностью разработанного олинцида к РНК-мишени, так как известно, что он несовершенно комплементарен, и для имеющихся в GenBank представителей семейства Triozidae он совпадает только на 10 из 11 нуклеотидов. По-видимому, несовершенная комплементарность с РНК-мишенью даже в один нуклеотид существенно снижает инсектицидное действие антисмыслового олигонуклеотида. Как и ожидалось, случайный фрагмент Слог-11 не проявил инсектицидного эффекта. Смертность от олигонуклеотида Слог-11 соответствует естественной смертности в контроле (рис. 2).
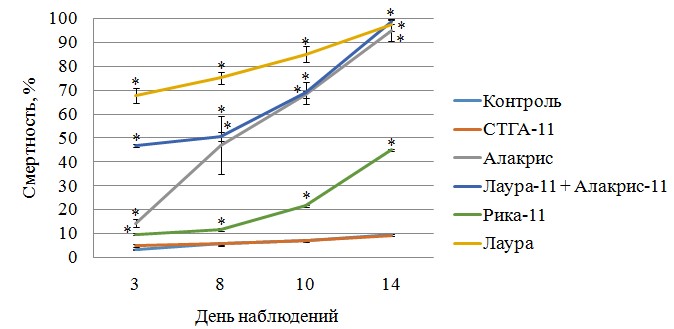
Рис. 2. Динамика смертности личинок лавровой листоблошки в эксперименте с различными олигонуклеотидами
* – достоверное различие по сравнению с контрольной группой (p<0,05).
В ходе эксперимента была оценена экспрессия предшественника полицистронной рРНК, содержащей внутренний транскрибируемый спейсер ITS2 (табл. 2). На третий день эксперимента наблюдалась сверхэкспрессия РНК-мишени для всех примененных олинцидов. По сравнению с контролем экспрессия увеличилась в 3,20,1, 3,560,66 и 2,930,16 раз для олигонуклеотида Проф-11, олинцидов Лаура-11 и Алакрис-11 соответственно, а для смеси олинцидов Лаура-11 с Алакрис-11 в 5,520,13 раз. На восьмые сутки наблюдалась характерная картина действия антисмысловых олигонуклеотидов со снижением экспрессии, кроме варианта Алакрис-11, у которого экспрессия была повышена в 1,350,01 раза по сравнению с контролем. На десятые сутки экспрессия в группе Алакрис-11 уменьшилась до 0,920,03 раз и практически сравнялась с контролем, тогда как у Проф-11 она возросла в
Новиков И. А., Яцкова Е. В., Шармагий А. К., Пузанова Е. В., Билык А. И., Оберемок В. В.
1,350,06 раза. На четырнадцатый день характерная картина снижения экспрессии наблюдалась только у Лаура-11 и смеси Лаура-11 с Алакрис-11, тогда как для Алакрис-11 и Проф-11 снова наблюдалась сверэкспрессия в 6,980,2 и 7,190,19 раз соответвтвенно. Все колебания уровня экспрессии в эксперименте имеют достоверное различие по сравнению с контрольной группой (p<0,05) (табл. 2). Для антисмысловых олигонуклеотидов понижение экспрессии целевого гена является «золотым» стандартом (Dias, Stein, 2002; Oberemok et al.,
2019; Gal’chinsky et al., 2020; Useinov et al., 2020), однако ранее нами были зафиксированы случаи увеличение экспрессии рибосомальных генов в ответ на применение ДНКинсектицидов у других видов насекомых. По-видимому, рибосомальные гены гиперкомпенсируют свою экспрессию в ответ на применение антисмысловых олигонуклеотидов, приводящих к нарушению функционирования клеток.
Таблица 2 Относительная концентрация РНК-мишени в личинках Trioza alacris после обработки ДНКолигонуклеотидами (контроль, относительно которого определялась достоверность разницы концентрации, принят за единицу)
| День эксперимента | Концентрация РНК-мишени | |||
| Проф-11 | Лаура-11 | Алакрис-11 | Лаура-11 и Алакрис-11 (1:1) | |
| Третий | 3,20,1 | 3,560,66 | 2,930,16 | 5,520,13 |
| Восьмой | 0,560,05 | 0,210,01 | 1,350,01 | 0,640,02 |
| Десятый | 1,350,06 | 0,0040,0001 | 0,920,03 | 0,010,0004 |
| Четырнадцатый | 6,980,21 | 0,580,05 | 7,190,19 | 0,00030,00002 |
Примечание к таблице. Все приведенные в таблице значения достоверно отличаются от контроля, p<0,05.
ЗАКЛЮЧЕНИЕ
В ходе исследования были разработаны, синтезированы и испытаны в полевых условиях олинциды Алакрис-11 и Лаура-11, показавшие высокую эффективность в исследовательских опытных группах на четырнацатый день поле обработки в дозировке 100 мг/л. Также исследован инсектицидный потенциал смеси данных олинцидов в соотношении 1:1, показавшей лучший результат из всех вариантов опыта также на четырнацатый день и составил 98,721,14 %. При помощи случайного фрагмента Слог-11 была продемонстрирована избирательность олинцидов, заключающаяся в отсутствии заметного эффекта на лавровую листоблошку. Также было показано, что частичная комплементарность олигонуклеотида оказывает существенно меньший инсектицидный эффект на целевое насекомое. Результаты экспериментов показывают безопасность олинцидов для нецелевых объектов и предоставляют уникальную возможность создавать таргетные препараты для конкретного вида насекомого, используя данные о геномных последовательностях вредителей. Нужно отметить, что в ответ на применение антисмысловых олигонуклеотидов наблюдалась преимущественно гиперкомпенсация содержания РНК-мишени на третий день после обработки, которая тем не менее приводила к гибели насекомого. Полученные результаты показывают перспективность создания безопасных и эффективных олигонуклеотидных инсектицидов для контрля численности насекомых-вредителей из подотряда Sternorryncha.
Работа выполнена в рамках проекта РНФ по теме «Разработка олигонуклеотидных инсектицидов для защиты растений против насекомых-вредителей из подотряда Грудохоботные (отряд Полужесткокрылые) на основе коротких антисмысловых олигонуклеотидов рибосомальных генов», № 22-16-20052.
166
Список литературы
Трикоз Н. Н. Основные вредители лавра благородного (Laurus nobilis L.) в парках Крыма и меры борьбы с ними // Бюллетень Государственного Никитского ботанического сада. – 2017. – № 124. – С. 116122.
Dias N., Stein C. A. Antisense oligonucleotides: Basic concepts and mechanisms // Molecular Cancer Therapeutics. – 2002. – Vol. 1, N 5. – P. 347–355.
Flor, G. Zur Kenntniss der Rhynchoten // Bulletin de la Société des Naturalistes de
Moscou. 1861. Vol. 34. Р. 331422.
Gal’chinsky N., Useinov R., Laikova K., Novikov I., Gorlov M., Plugatar Y., Oberemok V. A breakthrough in the efficiency of contact DNA insecticides: rapid high mortality rates in the sap-sucking insects Dynaspidiotus britannicus
Comstock and Unaspis euonymi Newstead // Journal of Plant Protection Research. 2020. Vol. 60. P. 220223.
MarmurJ., Doty P. Determination of the base composition of deoxyribonucleic acid from its thermal denaturation temperature // Journal of molecular biology. 1962. Vol. 5. P. 109118.
Novikov I. A., Yatskova E. V., Useinov R. Z., Gal’chinsky N. V., Puzanova Y. V., and V. V. Oberemok. Efcient Bay Sucker (Trioza alacris) Control with DNA Insecticides // Plant Posters. In Vitro Cell. Dev. Biol. Animal. –2022. Vol. 58 (Suppl 1). Р. 38–43. Oberemok V., Laikova K., Gal’chinsky N., Useinov R., Novikov I.,Temirova Z., Shumskykh M., Krasnodubets A., Repetskaya A., Dyadichev V., Fomochkina I., Bessalova E., Makalish T., Gninenko Y., Kubyshkin A. DNA insecticide developed from the Lymantria dispar 5.8S ribosomal RNA gene provides a novel biotechnology for plant protection // Scientific Reports. 2019. Vol. 9, N 1. P. 6197.
Oberemok V., Laikova K., Useinov R., Gal’chinsky N., Novikov I., Gorlov M. High Mortality of Sap-sucking Insects One Week After Topical Application of DNA Insecticides // In vitro biology meeting, San-Diego, June 4. 2020.
Paparella A., Nawade B., Shaltiel-Harpaz L., Ibdah M. A Review of the Botany, Volatile Composition, Biochemical and Molecular Aspects, and Traditional Uses of Laurus nobilis // Plants. – 2022. Vol. 9, N 11. – Р. 1209.
Psyl’list The World Psylloidea Database [Электронный ресурс]. – 2022. – Режим доступа: http://www.hemiptera-databases.com/psyllist (просмотрено 09.11.2022).
Useinov R., Gal’chinsky N., Yatskova E., Novikov I., Puzanova Y., Trikoz N., Sharmagiy A., Plugatar Y., Laikova K., Oberemok V. To bee or not to bee: creating DNA insecticides to replace non-selective organophosphate insecticides for use against the soft scale insect Ceroplastes japonicus Green // Journal of Plant Protection Research. 2020. Vol. 60, N 4. P. 406409.
Zoran P. Zeković, Žika D. Lepojević, Ibrahim O. Mujić. Laurel Extracts Obtained by Steam Distillation, Supercritical Fluid andSolvent Extraction // Journal of Natural Products. – 2009. – Vol. 2. – P. 104109.
Novikov I. A., Yatskova E. V., Sharmagiy A. K., Puzanova E. V., Bilyk A. I., Oberemok V. V. An innovative post-genomic approach for bay sucker control (Trioza alacris Flor.) // Ekosistemy. 2022. Iss. 31. P. 163–167.
In this article, we describe the effectiveness of oligonucleotide insecticides (DNA insecticides) Alacris-11 and Laura11, as well as their mixture in a 1:1 ratio, created to regulate the number of bay suker (Trioza alacris Flor.), which are based on short unmodified antisense DNA oligonucleotides that target ITS2 between 5.8S rRNA and 28S rRNA and 28S rRNA itself. The experiment was conducted with plants of the Laurus nobilis L. on the Southern coast of Crimea in 20212022 in three replicates. Significant insect mortality was noted on the third day of the experiment for the oligonucleotide insecticide Laura-11, which was 67.61±3.09 %. The maximum insect mortality was observed on the fourteenth day of the experiment and it was 95.00±4.42 % for Alacris-11 97.16±2.49 % for Laura-11 and 98.72±1.14 % for their mixture. After treatment with oligonucleotides, an unusual increase in the expression of the target RNA was detected on the third day of the experiment. For the target oligonucleotide insecticide Alacris-11, an increase in expression was also observed on the remaining days of the experiment. The maximum expression excess of 7.190.19 times was detected on the fourteenth day of the experiment for this oligonucleotide insecticide. Control fragment Prof-11 also caused mortality of the bay sucker, but it was low and on the fourteenth day was 45.08±0.41 %. The maximum increase in the expression level of the polycistroner RNA precursor transcript containing the intergenic transcribed spacer ITS2 after the use of Prof-11 was observed on the fourteenth day of the experiment and it was 6.980.21 times greater than in the controlsample. The absence of insecticidal activity of the control unmodified oligonucleotide Slog-11 indicates the selectivity of the action of oligonucleotide insecticides.
Key words: antisense DNA, oligonucleotide insecticides, Trioza alacris, bay sucker, Laurus nobilis, noble laurel, plant protection.
Поступила в редакцию 09.11.22 Принята к печати 23.11.22

